Азотни оксиди
Азотни оксиди се бинарни соединенија на кислород и азот или нивните соединенија. Азотот образува повеќе оксиди во кои оксидациониот број на азотот може да биде +1, +2, +3, +4 или +5, а формулите на оксидите се: N2O, NO, N2O3, NO2 и N2O5[1] Поважни азотни оксиди се:
- Азотен моноксид (NO), азот(II) оксид
- Азотен диоксид (NO2), азот(IV) оксид
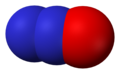
- Диазотен оксид (N2O), азот (I) оксид
- Диазотен триоксид (N2O3), азот(II, IV) оксид, анхидрид на азотастната киселина.
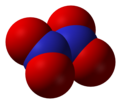
- Диазотен тетроксид (N2O4), азот(IV) оксид
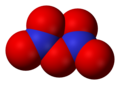
- Диазотен пентоксид (N2O5), азот(V) оксид, анхидрид на азотната киселина
(Последните три од спискот се нестабилни соединенија.)
Азот диоксидот може да се димеризира, образувајќи диазот тетраоксид. Диазот моноксидот е индиферентен оксид и нема значење доколку не станува збор за азотната киселина. Азот моноксидот не реагира со вода, но лесно се оксидира до азот диоксид, кој, пак, при растворањето во вода се диспропорционира, т.е. делумно се оксидира, а делумно се редуцира. Оттука, азот диоксидот може да се смета за мешан анхидрид на азотестата и азотната киселина.[2]
Хемиската реакција која доведува до создавање на азотните оксиди може да се произведe од неколку различни соединенија на кислород и азот (различни пропорционални односи), во зависност од условот на самата реакција. Ова е единствена причина зошто се споредни нус-производите со N2O; производството на останатите две стабилни оксиди на азот, кои се патем многу токсични, е регулирано со закон.
-
Азотен моноксид, NO -
Азотен диоксид, NO2 -
Диазотен оксид, N2O -
Диазотен триоксид, N2O3 -
Диазотен тетроксид, N2O4 -
Диазотен пентоксид, N2O5
NOx[уреди | уреди извор]
NOx е воопштена форма за моно-азотни оксиди (NO и NO2). Овие оксиди настануваат за време на процесот согорување, најчесто за време на процесот согорување на високи температури.[3][4]
На нормална, амбиентална температура кислородот и азотот не реагираат меѓусебно. За време на работата на мотор со внатрешно согорување, мешавината на воздухот и горивото произведуваат доволно висока температура за да се предизвика ендотермна реакција на атмосферскиот азот и кислородот во пламенот. Во градовите каде што сообраќајот е густ, количината на азотни оксиди е зголемена и може да биде дури и штетна.
Во присуство на повеќе кислород (O2), азотниот моноксид (NO) ќе реагира и ќе настане азотен диоксид (NO2), а временскиот период на овие реакции зависи од самата концентрација во воздухот, што може да се види од табелата:[5]
| NO концентрација во воздухот
(ppm) |
Време потребно половина од присутниот NO
да оксидира во NO2 (мин) |
|---|---|
| 20,000 | 0.175 |
| 10,000 | 0.35 |
| 1,000 | 3.5 |
| 100 | 35 |
| 10 | 350 |
| 1 | 3500 |
Кога -x и некои од органските испарливи смеси се (VOC) заедно во воздухот и во присуство на сончева светлина, тие формираат фотохемиски смог, кој создава голем дел од загадувањето на природата. Овие загадувања негативно влијаат врз човековото здравје[6].
1. Азотен диоксид, ако се раствори во влага од воздухот, формира компонента (азотна киселина) кисел дожд:
- 2NO2 + H2O → HNO2 + HNO3
(Азотен диоксид + вода → азотеста киселина + азотна киселина).
2. Потоа азотната киселина се разложува на:
- 3HNO2 → HNO3 + 2NO + H2O
(азотаста киселина → азотна киселина + азотен моноксид + вода),
3. каде што азотниот моноксид реагира со кислородот, оксидира и формира азотен диоксид кој повторно реагира со водата и повторно прави азотна киселина:
- 4NO + 3O2 + 2H2O → 4HNO3
(азотен моноксид + кислород + вода → азотна киселина).
Азотниот моноксид исто така учествува во создавањето озонска дупка во тропосферата.[7]
Биогенетичко потекло[уреди | уреди извор]
Во земјоделството употребата на минерални ѓубрива и збогатувањето на земјиштето со азотно ѓубриво исто така помага за збогатување на атмосферските NOx, преку процесот денитрификација на активните материи од минералното ѓубриво со помош на микроорганизмите кои го забрзуваат на процесот.[8][9]
Наводи[уреди | уреди извор]
- ↑ Бојан Шоптрајанов, Хемија за втора година на реформираното гимназиско образование (петто изменето и дополнето издание). Скопје: Просветно дело, 2009, стр. 132.
- ↑ Бојан Шоптрајанов, Хемија за втора година на реформираното гимназиско образование (петто изменето и дополнето издание). Скопје: Просветно дело, 2009, стр. 132-133.
- ↑ Lide, David R., уред. (2006). CRC Handbook of Chemistry and Physics (87. изд.). Boca Raton, FL: CRC Press. ISBN 0-8493-0487-3.
- ↑ Предлошка:Merck13th
- ↑ „NOx Removal“. Branch Environmental Corp. Архивирано од изворникот на 2007-10-08. Посетено на 26 декември 2007.
- ↑ „Health and Environmental Impacts of NOx“. United States Environmental Protection Agency.
- ↑ D. Fowler; и др. (1998). „The atmospheric budget of oxidized nitrogen and its role in ozone formation and deposition“. New Phytologist. 139: 11–23. doi:10.1046/j.1469-8137.1998.00167.x.
- ↑ J.N. Galloway; и др. (2004). „Nitrogen cycles: past, present, and future“. Biogeochemistry. 70 (2): 153–226. doi:10.1007/s10533-004-0370-0.
- ↑ E.A. Davidson & W. Kingerlee (1997). „A global inventory of nitric oxide emissions from soils“. Nutrient Cycling in Agroecosystems. 48: 37–50. doi:10.1023/A:1009738715891.